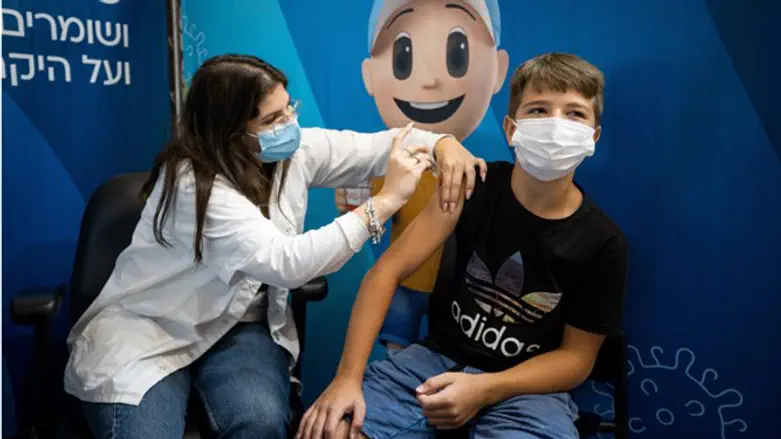
В понедельник компания Pfizer-BioNTech объявила, что ее вакцина от COVID-19 доказала свою безопасность и эффективность в ходе клинических испытаний фазы 2/3 для детей в возрасте от 5 до 11 лет.
В исследовании использовалась схема приема двух доз по 10 мкг с интервалом 21 день, что меньше, чем доза 30 мкг, применяемая для людей от 12 лет и старше. Ответы антител у участников, получавших дозы 10 мкг, были сопоставимы с таковыми, зарегистрированными в предыдущем исследовании Pfizer-BioNTech у людей в возрасте от 16 до 25 лет, иммунизированных дозами 30 мкг. Доза 10 мкг была тщательно выбрана как предпочтительная доза с точки зрения безопасности, переносимости и иммуногенности у детей от 5 до 11 лет. Это первые результаты основного испытания вакцины COVID-19 в этой возрастной группе.
«За последние девять месяцев сотни миллионов людей в возрасте от 12 лет и старше со всего мира получили нашу вакцину от COVID-19. Мы стремимся расширить защиту, обеспечиваемую вакциной, на это более молодое население, при условии получения разрешения регулирующих органов, особенно поскольку мы отслеживаем распространение варианта Delta и серьезную угрозу, которую он представляет для детей», - сказал Альберт Бурла, председатель и главный исполнительный директор Pfizer.
«С июля количество случаев заболевания COVID-19 у детей в США возросло примерно на 240 процентов, что подчеркивает необходимость вакцинации для общественного здравоохранения. Эти результаты испытаний обеспечивают прочную основу для получения разрешения на нашу вакцину для детей в возрасте от 5 до 11 лет, и мы планируем срочно представить их в FDA и другие регулирующие органы».
«Мы рады, что можем предоставить данные регулирующим органам для этой группы детей школьного возраста до начала зимнего сезона», - сказал д-р Угур Сахин, генеральный директор и соучредитель BioNTech.
«Профиль безопасности и данные об иммуногенности у детей в возрасте от 5 до 11 лет, вакцинированных более низкой дозой, согласуются с теми, которые мы наблюдали с нашей вакциной в других пожилых популяциях при более высокой дозе».
Обобщенные данные этого исследования фазы 2/3, в котором участвуют дети в возрасте от 6 месяцев до 11 лет, были для 2 268 участников в возрасте от 5 до 11 лет, получивших дозу 10 мкг по схеме с двумя дозами. В испытании средний геометрический титр нейтрализующих антител SARS-CoV-2 (GMT) составлял 1197,6 (95% доверительный интервал [CI, 1106,1, 1296,6]), что свидетельствует о сильном иммунном ответе в этой когорте детей через месяц после второй дозы. Это сравнимо с GMT 1146,5 (95% ДИ: 1045,5, 1257,2 для участников в возрасте от 16 до 25 лет, использованных в качестве контрольной группы для этого анализа и которым вводили схему с двумя дозами 30 мкг. Кроме того, вакцина COVID-19 хорошо переносилась, а побочные эффекты в целом были сопоставимы с теми, которые наблюдались у участников в возрасте от 16 до 25 лет.
Pfizer и BioNTech планируют как можно скорее поделиться этими данными с Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA), Европейским агентством по лекарственным средствам (EMA) и другими регулирующими органами, говорится в заявлении компаний.
Что касается Соединенных Штатов, компании рассчитывают включить данные в краткосрочную заявку на разрешение на использование в чрезвычайных ситуациях (EUA), поскольку они продолжают накапливать данные о безопасности и эффективности, необходимые для подачи на полное одобрение FDA в этой возрастной группе. Запланирован также запрос в EMA об обновлении условного регистрационного удостоверения ЕС.
Считывание показаний верхних линий для двух других возрастных групп из исследования - детей от 2 до 5 лет и детей от 6 месяцев до 2 лет - ожидается не ранее четвертого квартала этого года.
Pfizer и BioNTech планируют предоставить данные полного испытания фазы 3 для научной рецензируемой публикации.
Ранее на этой неделе FDA одобрило бустерную дозу вакцины Pfizer-BioNTech только для тех, кто старше 65 лет или иным образом определен как группа высокого риска, несмотря на израильские данные, показывающие, что третья доза обеспечивает в 10 раз большую защиту, чем первые две.
В прошлом месяце сообщалось, что более 500 израильских детей в возрасте от 5 до 11 лет получили вакцину Pfizer-BioNTech, несмотря на то, что она не была одобрена для их возрастной группы.
Эти дети относились к категориям повышенного риска и были специально отобраны Министерством здравоохранения для вакцинации. На момент публикации сообщений о необычных побочных эффектах не поступало; единственными побочными эффектами были обычные легкие симптомы, ожидаемые после вакцинации.